Merkillepantavaa on,
että vaikka lymfoomien
diagnostiikan perustana
säilyvät edelleen potilaan
kliininen kuva, tautisolujen
morfologia (perifeerinen veri,
luuydinaspiraatio ja
histologiset näytteet),
kudoksen perusrakenne ja
immunohistokemialliset (IHC)
tutkimukset, kasvaa
molekyyligeneettisten
menetelmien osuus ja
tulee joissakin taudeissa
pakolliseksi.
3/2017 Moodi 39
PATOLOGIA
WHO:n lymfoomaluokitus uudistuu
Jatkuu seuraavalla sivulla
SAMULI VAITTINEN
on lääketieteen tohtori ja
patologian erikoislääkäri,
joka toimii Tyks-Sapaliikelaitoksen
patologian
palvelualueella.
Päivitettyyn tietoon pohjautuva, toimiva
ja hyvin toistettavissa oleva tautiluokitus
on lääketieteen kulmakivi.
Taudit on kuvailtava ja niiden kriteerit
määriteltävä tarkasti, jotta niitä
voidaan diagnosoida, hoitaa ja tutkia. Maailman
terveysjärjestön (World Health Organization,
WHO) hematopoieettisten ja lymfaattisten
kudosten kasvainten luokitus uudistuu tänä
vuonna. Uudistettua WHO:n luokitusta ovat
yhteistyössä tehneet patologit, hematologit,
onkologit ja geneetikot. Tavoitteena on saada
aikaan luokitus, joka vastaisi paitsi diagnostisen,
myös kliinisen työn tarpeisiin.
Vanha vuoden 2008 ”Sinisen kirjan” 4. painos
saa vuoden 2016 päivityksen. Kirjaa ei
ole vielä julkaistu, mutta sen on luvattu ilmestyvän
vuoden 2017 aikana. Periaatteellisesti
kyseessä ei ole kuitenkaan varsinainen uusi
luokitus, vaan vanhan 4. painoksen päivitys,
sillä WHO:n tautiluokituksessa muiden tuumorien
monografioiden osalta ei ole päästy
kaikilta osin 4. painokseen saakka. Päivityksessä
huomioidaan kuluneen kahdeksan vuoden
aikana kertynyttä tietoa niin diagnostiikan,
hoidon kuin ennusteenkin suhteen. Vuoden
2016 päivityksessä osa vanhoista väliaikaisistaentiteeteistä
muuttuu vakiintuneiksi,
ja uusia väliaikaisia entiteettejä otetaan entiteettejä
otetaan mukaan. Lisäksi tulee joitakin
nimikkeiden muutoksia, mutta varsinaisia
täysin uusia vakiintuneita entiteettejä ei mukana
ole.
Merkillepantavaa on, että vaikka lymfoomien
diagnostiikan perustana säilyvät edelleen
potilaan kliininen kuva, tautisolujen morfologia
(perifeerinen veri, luuydinaspiraatio
ja histologiset näytteet), kudoksen perusrakenne
ja immunohistokemialliset (IHC) tutkimukset,
kasvaa molekyyligeneettisten menetelmien
osuus ja tulee joissakin taudeissa pakolliseksi.
Uusia mutaatioita on löydetty niin
lymfoomista kuin myeloproliferatiivisista ja
-dysplastisista sairauksistakin, ja niiden vaikutusta
ennusteeseen ja hoitoon korostetaan
nyt myös diagnostiikassa.
Merkittävimmistä muutoksista on julkaistu
katsausartikkelit Blood-lehdessä 2016.
Seuraavassa tarkastelen käytännön kannalta
oleellisimpia muutoksia keskittyen B-solulymfoomiin,
koska nämä ovat yleisimpiä lymfoomia,
ja niiden osalta tulee joitakin oleellisia
muutoksia diagnostiikkaan. Lyhyesti
käyn läpi myös T-solulymfoomiin tulevia
muutoksia. Hodgkinin lymfooman luokitus
pysyy oleellisesti ennallaan aiempaan nähden,
joten sen jätän artikkelin ulkopuolelle.
Myös myelodysplastisten ja -proliferatiivisten
tautien luokitukseen tulee joitakin muutoksia,
mutta tilanpuutteen vuoksi nekin jätetään
tämän artikkelin ulkopuolelle. Osa tässä
tekstissä mainituista muutoksista saattaa vielä
tarkentua, kun kirja lopulta julkaistaan kokonaisuudessaan.
Diff uusi suurisoluinen
B-solulymfooma (DLBCL) ja
High-grade lymfoomat (HGBL)
Diffuusi suurisoluinen B-solulymfooma (DLBCL)
on yleisin lymfooma Suomessa ja maailmalla.
Tämä jaetaan ”not otherwise specified”
(NOS) -alatyyppiin sekä muutamiin muihin
morfologisesti tai kliinisesti erityisiin ryhmiin,
kuten esim. primaariseen mediastinaaliseen
tai T-solu/histiosyyttirikkaaseen muotoon.
NOS-alatyyppi on oikeastaan ns. roskakoppadiagnoosi,
johon luokittuvat taudit, jotka
eivät muihin alatyyppeihin sovi. Siksi DLBCL,
NOS on varsin heterogeeninen tautiryhmä.
Jo 2008 luokituksessa mainitaan DLBCL,
NOS -jaottelu kahteen solun alkuperän suhteen
erilaiseen alaryhmään: itukeskusperäisiin
(germinal center B-cell, GCB) ja aktivoitunut
B-solu-peräisiin (activated B-cell, ABC/
non-GCB). Tämä jaottelu tulee 2016 päivityksessä
pakolliseksi. Näillä kahdella alatyypillä
on erilainen ennuste ja hoitokäytännötkin
ovat ilmeisimmin muuttumassa, jonka vuoksi
tyypitys on tarpeellinen. Tietojeni mukaan
jaottelu onkin jo Suomessa käytössä ainakin
kaikissa yliopistosairaaloissa, joten tämä ei
sinänsä tuo oleellista muutosta nykykäytäntöön.
Jaottelun voi edelleen tehdä joko immunohistokemiallisesti
tai geeniekspressioprofiloinnilla
(GEP), joista edellisen saatavuus on
oleellisesti parempi. Yleisimmin immunohistokemiallisesti
käytetty menetelmä on Hansin
luokitus, mutta muutkin algoritmit ovat sallittuja.
Hansin luokitus tehdään kolmella vas-
Pahanlaatuiset veritaudit Suomessa 2014
Hodgkinin lymfooma
5 %
B-soluinen
KLL/pienilymfosyy��nen
lymfooma
11 %
Man��elisolulymfooma
3 %
Follikulaarinen lymfooma
7 %
Diffuusi suurisoluinen Bsolulymfooma
Burki��n 19 %
lymfooma/leukemia
1 %
Marginaalivyöhykkeen
lymfooma
3 %
Kypsät T- ja NKsolukasvaimet
3 %
Muut
35 %
Myelooma ja muut
plasmasolutaudit
13 %
Hodgkinin lymfooma
B-soluinen KLL/pienilymfosyy��nen lymfooma
Man��elisolulymfooma
Follikulaarinen lymfooma
Diffuusi suurisoluinen B-solulymfooma
Burki��n lymfooma/leukemia
Marginaalivyöhykkeen lymfooma
Kypsät T- ja NK-solukasvaimet
Myelooma ja muut plasmasolutaudit
Muut
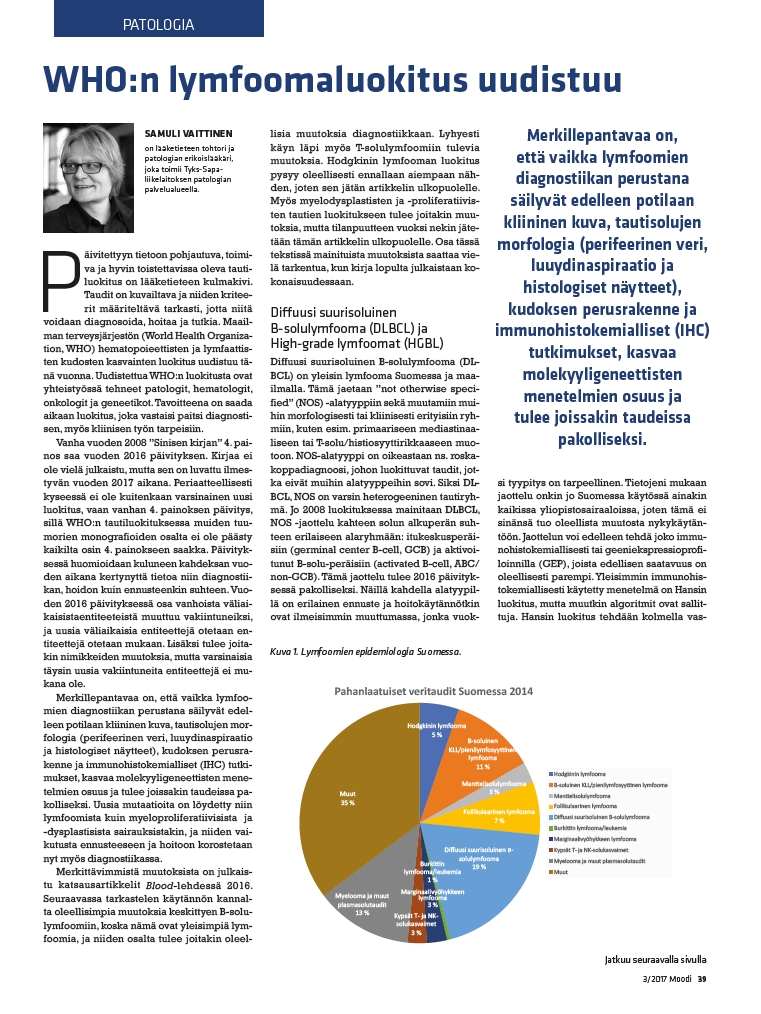
Kuva 1. Lymfoomien epidemiologia Suomessa.